Перейти к:
Определение безопасности биорезорбируемого имплантата на основе полилактат-когликолида в эксперименте
https://doi.org/10.46563/1560-9561-2025-28-2-114-118
EDN: drukte
Аннотация
Введение. Лечение переломов костей с нарушением зоны роста у детей является актуальной задачей. Около- и внутрисуставные переломы являются частым повреждением опорно-двигательного аппарата у детей. Однако нерешённым остаётся вопрос выбора безопасного фиксатора.
Цель работы: определить безопасность биорезорбируемого имплантата на основе полилактат-когликолида (ПЛГА) для хирургического лечения дистального метаэпифизеолиза большеберцовой кости у детей.
Материалы и методы. Работа выполнена на 120 белых крысах в возрасте 3 мес, массой 110–120 г. Животные были распределены на 2 группы: основную группу составили 100 крыс, по 50 самок и самцов. Животным этой группы внутрибрюшинно были имплантированы фрагменты биополимера ПЛГА. Заживление происходило естественным путём. Контрольная группа состояла из 20 крыс, по 10 самок и самцов, этим животным имплантация биополимера не производилась. Наблюдение осуществляли в течение 3 мес от даты имплантации.
Результаты. Имплантат на основе ПЛГА не оказывал негативного влияния на состояние животных, признаков воспаления не отмечено. Через 3 мес имплантат разрушался в брюшной полости животных. Значимых отклонений в состоянии животных, снижении массы их тела, изменений в анализах крови не выявлено.
Заключение. Биополимер на основе ПЛГА может использоваться в качестве биорезорбируемого фиксатора при около- и внутрисуставных переломах костей.
Для корреспонденции: Серова Наталья Юрьевна,
Участие авторов:
Серова Н.Ю., Яцык С.П., Челпаченко О.Б., Артифексова А.А. — концепция и дизайн исследования;
Серова Н.Ю., Лушников А.М. — сбор и обработка материала, статистическая обработка материала;
Серова Н.Ю., Челпаченко О.Б. — написание текста;
Серова Н.Ю., Челпаченко О.Б., Артифексова А.А. — научное редактирование.
Все соавторы — утверждение окончательного варианта статьи, ответственность за целостность всех частей статьи.
Финансирование. Исследование не имело финансовой поддержки.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Поступила 04.03.2025
Принята к печати 18.03.2025
Опубликована 29.04.2025
Ключевые слова
Для цитирования:
Серова Н.Ю., Челпаченко О.Б., Яцык С.П., Никишов С.О., Лушников А.М., Артифексова А.А. Определение безопасности биорезорбируемого имплантата на основе полилактат-когликолида в эксперименте. Российский педиатрический журнал. 2025;28(2):114-118. https://doi.org/10.46563/1560-9561-2025-28-2-114-118. EDN: drukte
For citation:
Serova N.Yu., Chelpachenko O.B., Yatsyk S.P., Nikishov S.O., Lushnikov A.M., Artifeksova A.A. Experimental determination of the safety of bioresorbable polylactate-coglycolide-based implants. Russian Pediatric Journal. 2025;28(2):114-118. (In Russ.) https://doi.org/10.46563/1560-9561-2025-28-2-114-118. EDN: drukte
Введение
В последние годы достигнут значительный прогресс в разработке хирургических технологий остеосинтеза костей скелета с применением биорезорбируемых имплантатов [1, 2]. Подобные имплантаты используются в травматологии в качестве штифтов и винтов и позволяют исключить дополнительные вмешательства по удалению имплантата [3]. Полимерные фиксаторы, как правило, изготовлены на основе полимолочной кислоты, не обладают остеогенной активностью, а заживление перелома происходит в обычные сроки [4, 5]. Возможность замещения различных металлоконструкций биодеградируемыми полимерами является актуальной темой в травматологии и ортопедии [5, 6]. Полимер молочно-гликолевой кислоты (ПЛГА) является известным биоразлагаемым материалом. Повышенный интерес травматологов к применению биодеградируемых имплантатов открыл для ПЛГА перспективное будущее при лечении переломов [7, 8]. Однако определение безопасности биодеградируемых имплантатов на основе ПЛГА для внедрения в практику детского травматолога ещё не проводилось в необходимом объёме.
Цель работы: определить безопасность биорезорбируемого имплантата на основе ПЛГА для хирургического лечения дистального метаэпифизеолиза большеберцовой кости у детей.
Материалы и методы
Эксперименты выполнены на лабораторных белых крысах. Содержание животных и все исследования с их участием проводили в строгом соответствии с современными стандартами по защите позвоночных животных, используемых для экспериментов и других научных целей. Эксперименты были проведены на 50 крысах-самках возрастом 3 мес (масса тела 110–120 г) и 50 самцах возрастом 3 мес (масса тела 100–120 г). Для контроля выбраны 20 животных обоих полов того же возраста и веса.
Основные периоды обследования регламентированы стандартами, относящимися к имплантации биостабильных материалов, которые в норме составляют 1–12 нед. Имплантацию фрагментов ПЛГА в брюшную полость животных проводили под лёгким эфирным наркозом: образцы вводили внутрибрюшинно по 20 штук, длина каждого фрагмента 0,5 см, диаметр 1,5 мм. Одновременно из вены хвоста животных осуществляли забор крови для анализа.
Все животные после операции проснулись, были активны. Лабораторные показатели определяли в начале эксперимента и затем в динамике через 1, 2 и 3 мес. При этом одновременно проводили общий анализ крови и биохимический анализ: общий белок, аланинаминотрансфераза, общая α-амилаза, мочевина, креатинин, глюкоза, холестерин, общий билирубин.
Тема работы и дизайн исследования были одобрены независимым локальным этическим комитетом.
Статистический анализ проводился с использованием программы «StatTech v. 4.7.1» («Статтех»). В случае отсутствия нормального распределения данные описывали с помощью медианы (Me) и нижнего и верхнего квартилей [Q1; Q3]. При сравнении нормально распределённых показателей, рассчитанных для двух связанных выборок, использовали парный t-критерий Стьюдента. При сравнении показателей, распределение которых отличалось от нормального, в двух связанных группах использовали критерий Вилкоксона. Различия считали значимыми при p < 0,05.
Результаты
У всех животных после внутрибрюшинного введения имплантатов на основе ПЛГА общее состояние было удовлетворительным. Не выявлено изменений функционирования основных систем организма животных. Никаких нарушений в питании, выпаивании, наличии инфекционных болезней или неврологических отклонений у животных не отмечено. Клиническая картина соответствовала нормальному поведению и состоянию животных. В движении и в покое животные имели физиологическое положение в пространстве. После введения имплантантов на основе ПЛГА у животных не выявлено значимых различий в динамике показателей общего анализа крови в начале опыта, через 1, 2 и 3 мес (табл. 1).
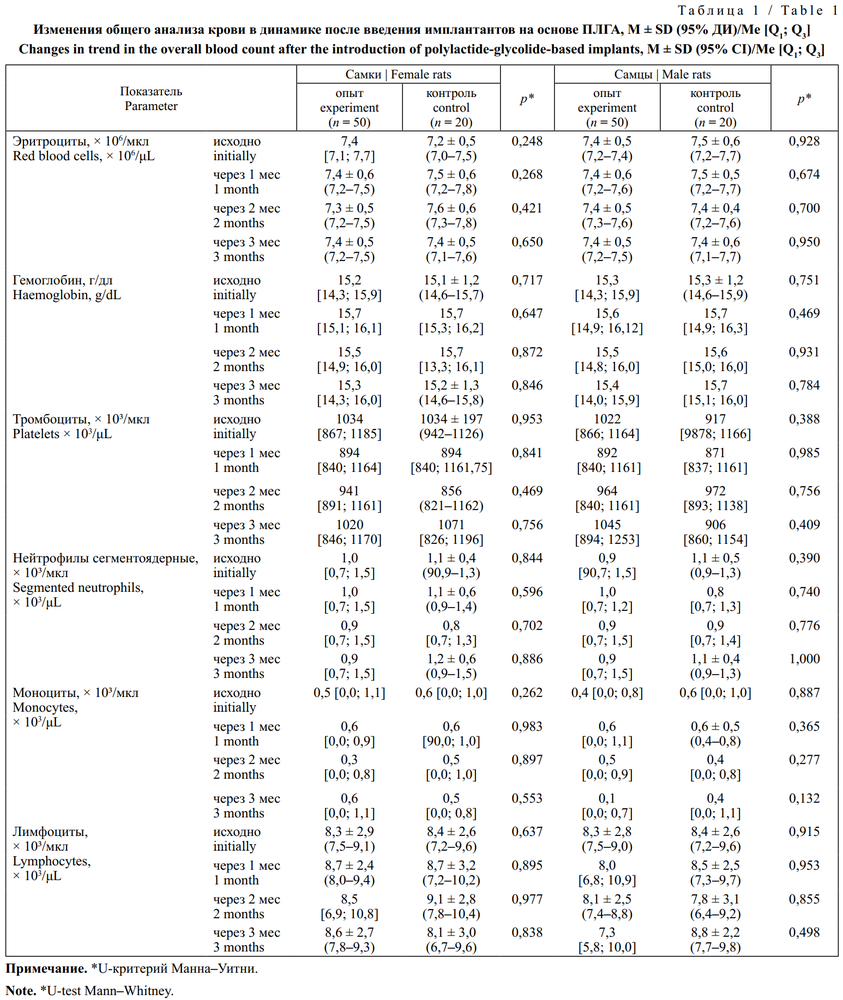
После имплантации фрагментов на основе ПЛГА животным биохимические показатели крови существенно не изменялись в начале опыта и динамике (табл. 2).
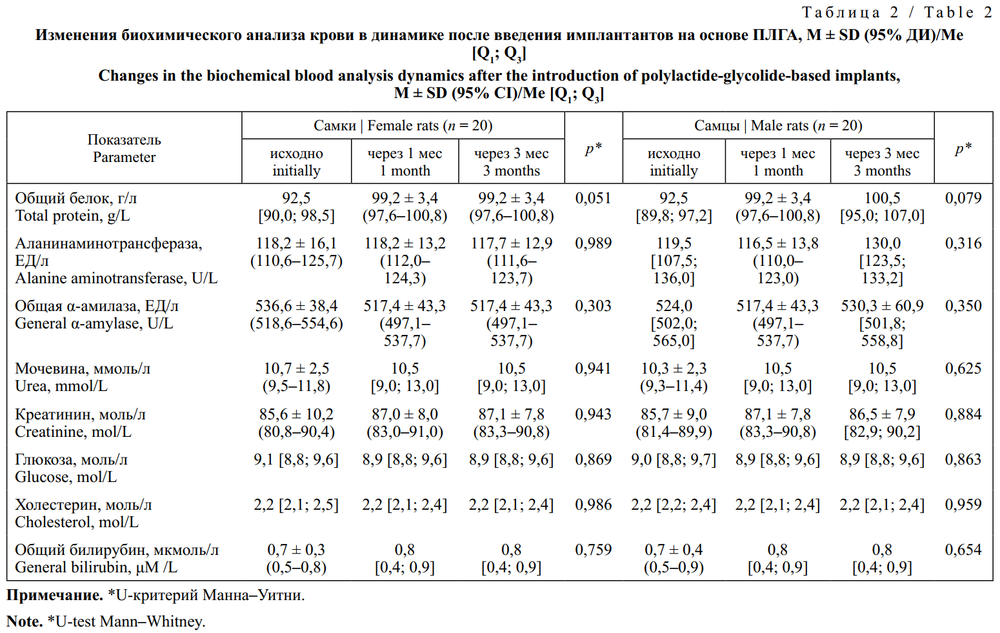
Таким образом, представленные данные свидетельствуют об отсутствии значимого влияния имплантатов на основе ПЛГА на состояние экспериментальных животных и их жизнедеятельность.
Обсуждение
Лечение переломов с повреждением зоны роста костей у детей, несомненно, является актуальной задачей для детской травматологии. Традиционно преобладает консервативное лечение переломов. Однако значимые смещения требуют закрытой репозиции. В тех случаях, когда не удаётся сохранить стояние отломков после закрытой репозиции, применяют металлоостеосинтез спицами с последующей гипсовой иммобилизацией. Однако пока не создан фиксатор с совместимой полимерной биодеградируемой структурой, не требующий удаления в последующем [3, 8]. Имеются полимеры без остеогенной активности с обычными сроками биодеградации полимеров: полилактат, поликапрон и ПЛГА [8, 9]. Однако работы для подтверждения биобезопасности и отсутствия токсичности имплантатов на основе ПЛГА в необходимом объёме не проводились.
В нашей работе после внутрибрюшинной имплантации животным фиксатора на основе ПЛГА их общее состояние и жизнедеятельность существенно не изменялись по сравнению с контролем. Двигательная активность, поведенческие реакции и масса тела животных не менялись в динамике по сравнению с контролем. При этом не выявлено значимых различий в общем и биохимическом анализах крови животных в начале опытов и в динамике через 1, 2 и 3 мес после введения имплантата на основе ПЛГА. Следовательно, доказаны отсутствие токсичности и биобезопасность имплантата на основе ПЛГА, что позволяет определить показания к возможному использованию биоразлагаемых фиксаторов в детской травматологии в зависимости от тяжести перелома. Вместе с тем очевидно, что имплантанты для травматологии должны быть достаточно охарактеризованы и протестированы, помимо требований о доказанной пользе для здоровья [10]. Широкое применение имплантатов на основе ПЛГА в качестве фиксаторов в детской травматологии возможно лишь после выполнения полного цикла регуляторных и экспериментальных исследований в соответствии со стандартами1. Для реализации этих требований необходимо проведение работ in vivo для определения эмбрио- и тератотоксичности и анализа возможного негативного влияния на зону роста костей в процессе взросления.
Несмотря на преимущества имплантатов на основе биорезорбируемых полимерных материалов, следует отметить их недостатки: прежде всего, это длительный срок деградации (ПЛГА — до 1,5–2,0 лет) по сравнению с периодом сращения и восстановления костных повреждений [11, 12]. Во время деградации биополимеров вокруг прилежащих тканей образуется кислая среда, что часто вызывает местную воспалительную реакцию и оказывает неблагоприятное воздействие на восстановление тканей [13]. Устранить перечисленные недостатки можно с помощью добавления к полимерной матрице резорбируемого дисперсного наполнителя (гидроксиапатит, трикальцийфосфат) [14]. Показано, что биокерамика обладает остеокондуктивностью, резорбтивными свойствами, уменьшает кислотность продуктов деградации [15].
Заключение
Биорезорбируемый имплантат на основе ПЛГА не оказывает значимого негативного воздействия на показатели жизнедеятельности экспериментальных животных. Внутрибрюшинное имплантирование фрагментов фиксаторов не влияет отрицательно на лабораторные показатели, что указывает на их биобезопасность при клиническом применении.
1ГОСТ Р ИСО 14630–2017. Имплантаты хирургические неактивные. М.; 2017.
Список литературы
1. Рошаль Л.М., Лушников А.М., Басаргин Д.Ю., Воробьёв Д.А., Никишов С.О. Применение биодеградируемых имплантов при лечении детей с около- и внутрисуставными переломами. Детская хирургия. 2018; 22(3): 116–9. https://elibrary.ru/xuzgkd
2. Дорохин А.И., Адрианова А.А., Худик В.И., Сорокин Д.С., Горюнов А.К. Особенности лечения детей с переломами дистального метаэпифиза костей голени: клинические наблюдения. Российский вестник детской хирургии, анестезиологии и реаниматологии. 2020; 10(4): 453–60. https://doi.org/10.17816/psaic717 https://elibrary.ru/vttlfs
3. Heye P., Matissek C., Seidl C., Varga M., Kassai T., Jozsa G., et al. Making hardware removal unnecessary by using resorbable implants for osteosynthesis in children. Children (Basel). 2022; 9(4): 471. https://doi.org/10.3390/children9040471
4. Резник Л.Б., Гурьев В.В., Турушев М.А., Негров Д.А., Ильин Р.Е. Остеосинтез авульсивных переломов у больных с различной минеральной плотностью костной ткани. Травматология и ортопедия России. 2018; 24(4): 72–80. https://doi.org/10/21823/2311-2905-2018-24-4-72-80 https://elibrary.ru/ysiixj
5. Терещенко В.П., Ларионов П.М., Кирилова И.А., Садовой М.А., Мамонова Е.В. Материалы и методы тканевой инженерии костной ткани. Хирургия позвоночника. 2016; 13(1): 72–81. https://doi.org/10.14531/ss2016.1.72-81 https://elibrary.ru/vqgegl
6. Тагандурдыева Н., Юдин В.Е. Биорезорбируемые композиты для костной пластики. Российские нанотехнологии. 2020; 15(4): 418–34. https://doi.org/10.1134/S1992722320040159 https://elibrary.ru/bejarl
7. Сиразетдинов А.В., Никифоров А.А., Вольфсон С.И. Полимерные композиционные материалы на основе полилактида. Каучук и резина. 2021; 80(6): 326–36. https://elibrary.ru/kjnqte
8. Хисамиева Д.Р., Шарафиев И.А., Агатиева Э.А., Никифоров А.А., Галимзянова Р.Ю., Ксембаев С.С. и др. Биорезорбируемые композиционные материалы для остеосинтеза: обзор современных исследований. Вестник современной клинической медицины. 2024; 17(1): 119–26. https://elibrary.ru/ghdttc
9. Luo Y., Wang J., Ong M.T.Y., Yung P.S., Wang J., Qin L. Update on the research and development of magnesium-based biodegradable implants and their clinical translation in orthopaedics. Biomater. Transl. 2021; 2(3): 188–96. https://doi.org/10.12336/biomatertransl.2021.03.003
10. Дурнев А.Д. Лекарственная токсикология занимает важнейшее место в структуре доклинических исследований. Ведомости Научного центра экспертизы средств медицинского применения. 2023; 13(1): 8–13. https://doi.org/10.30895/1991-2919-2023-13-1-8-13 https://elibrary.ru/ebzroo
11. Гайнетдинова А.А., Крупнин А.Е., Сорокин Ф.Д., Седуш Н.Г., Чвалун С.Н. Топологическая оптимизация моделей имплантатов для остеосинтеза костей предплечья на основе биоразлагаемых полимерных материалов. В кн.: XXX Международная инновационная конференция молодых ученых и студентов (МИКМУС – 2018). М.; 2019: 378–82. https://elibrary.ru/ywlejv
12. Zamora R., Jackson A., Seligson D. Correct techniques for the use of bioabsorbable implants in orthopaedic trauma. Curr. Orthop. Pract. 2016; 27(4): 469–73. https://doi.org/10.1097/BCO.0000000000000378
13. Kohn D.H., Sarmadi M., Helman J.I., Krebsbach P.H. Effects of pH on human bone marrow stromal cells in vitro: implications for tissue engineering of bone. J. Biomed. Mater. Res. 2002; 60(2): 292–9. https://doi.org/10.1002/jbm.10050
14. Taherimehr M., Bagheri R., Taherimehr M. In-vitro evaluation of thermoplastic starch/ beta-tricalcium phosphate nano-biocomposite in bone tissue engineering. Ceram. Int. 2021; 47(11): 15458–63. https://doi.org/10.1016/j.ceramint.2021.02.111
15. Wei S., Ma J.X., Xu L., Gu X.S., Ma X.L. Biodegradable materials for bone defect repair. Mil. Med. Res. 2020; 7(1): 54. https://doi.org/10.1186/s40779-020-00280-6
Об авторах
Наталья Юрьевна СероваРоссия
Ст. науч. сотр. отдела травматологии и медицины катастроф ГБУЗ «НИИ неотложной детской хирургии и травматологии — Клиника доктора Рошаля» ДЗМ
e-mail: serova_tu@yahoo.com, serovany@zdrav.mos.ru
Олег Борисович Челпаченко
Россия
Докт. мед. наук, гл. науч. сотр., лаб. научных основ нейроортопедии и ортопедии, проф. каф. детской хирургии с курсом анестезиологии и реанимации, врач — травматолог-ортопед нейроортопедического отделения с ортопедией ФГАУ «НМИЦ здоровья детей»; рук. отдела травматологии и медицины катастроф, врач — травматолог-ортопед консультативно-диагностического отделения, ст. преподаватель учебно-методического отдела ГБУЗ «НИИ неотложной детской хирургии и травматологии — Клиника доктора Рошаля» ДЗМ
e-mail: сhelpachenko81@mail.ru
Сергей Павлович Яцык
Россия
Докт. мед. наук, чл.-корр. РАН, проф. каф. детской хирургии им. акад. С.Я. Долецкого ФГБОУ ДПО РМАНПО
e-mail: makadamia@yandex.ru
Сергей Олегович Никишов
Россия
Канд. мед. наук, зав. отделением травматологии ГБУЗ «НИИ неотложной детской хирургии и травматологии — Клиника доктора Рошаля» ДЗМ
e-mail: nso.doc@yandex.ru
Александр Михайлович Лушников
Россия
Врач — травматолог-ортопед, отделение травматологии ГБУЗ «НИИ неотложной детской хирургии и травматологии — Клиника доктора Рошаля» ДЗМ
e-mail: lushnikov1981@yandex.ru
Анна Алексеевна Артифексова
Россия
Доктор мед. наук, проф., методист ГБУЗ НО «Медицинский информационно-аналитический центр»
e-mail: аrtifeksova@yandex.ru
Рецензия
Для цитирования:
Серова Н.Ю., Челпаченко О.Б., Яцык С.П., Никишов С.О., Лушников А.М., Артифексова А.А. Определение безопасности биорезорбируемого имплантата на основе полилактат-когликолида в эксперименте. Российский педиатрический журнал. 2025;28(2):114-118. https://doi.org/10.46563/1560-9561-2025-28-2-114-118. EDN: drukte
For citation:
Serova N.Yu., Chelpachenko O.B., Yatsyk S.P., Nikishov S.O., Lushnikov A.M., Artifeksova A.A. Experimental determination of the safety of bioresorbable polylactate-coglycolide-based implants. Russian Pediatric Journal. 2025;28(2):114-118. (In Russ.) https://doi.org/10.46563/1560-9561-2025-28-2-114-118. EDN: drukte





























